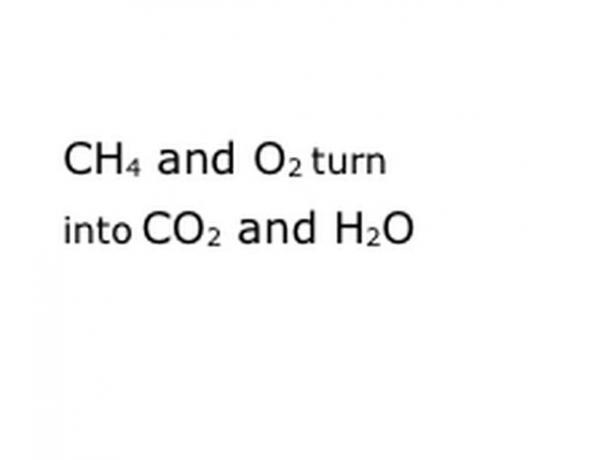
酢はあなたが家の周りで見つける最も有用な化学物質の1つです。 これは基本的に、化学式Cの酢酸の約5%の低濃度溶液です。2H4O2、CHと書かれることもあります3COOHは、緩く結合した水素イオンを分離して酸性にします。 pHが約2.4の酢酸はかなり腐食性がありますが、料理用酢の濃度が非常に低いため、フライドポテトやサラダに酢を注ぐのに問題はありません。 酢を使用した2つの実験室での実験では、発熱反応と吸熱反応を示すことができます。これらは、それぞれ熱を放出および吸収する反応です。 1つは、1つよりも多くの方法で冷える発泡火山を生成し、もう1つは錆びた金属といくらかの熱を生成します。
TL; DR(長すぎる; 読んでいない)
発熱反応は熱を発生し、吸熱反応は熱を消費します。 重曹と酢を混ぜて吸熱反応を目撃し、スチールウールを酢に浸して発熱反応を目撃します。
発泡火山実験
酢と重曹(重曹)を合わせて温度を測ると、約1分で摂氏約4度(華氏7.2度)下がる。 温度低下は酢とベーキングの間の特定の反応の結果ではありませんが ソーダ、あなたがそれらを組み合わせなければそれは起こらないでしょう、それで全体的なプロセスは吸熱として適格です 反応。 この組み合わせはまた、二酸化炭素ガスを放出し、それが混合物の内部で泡立ち、火山からの溶岩のように容器から上昇する泡を生成します。
この反応は2つのステップで発生します。 最初に、酢の酢酸は重曹と反応して酢酸ナトリウムと炭酸を生成します:
NaHCO3 + HC2H3O2 →NaC2H3O2 + H2CO3
炭酸は不安定で、すぐに分解して二酸化炭素と水を形成します。
H2CO3 →H2O + CO2
この式でプロセス全体を要約できます。
NaHCO3 + HC2H3O2 →NaC2H3O2 + H2O + CO2
つまり、重曹と酢酸は、酢酸ナトリウムと水と二酸化炭素を生成します。 炭酸分子を水と二酸化炭素に分解するためにエネルギーが必要なため、反応は熱を消費します。
錆びたスチールウールの実験
酸化反応は熱を発生するため発熱します。 ログの書き込みは、この極端な例を示しています。 錆は酸化反応であるため、熱を発生しますが、通常、熱の放散が速すぎて目立たなくなります。 ただし、スチールウールパッドをすぐに錆びさせることができれば、温度上昇を記録することができます。 これを行う1つの方法は、スチールウールパッドを酢に浸して、スチールファイバーから保護コーティングを取り除くことです。
細かいスチールウールのパッドをガラス容器に入れ、それを覆うのに十分な酢を注ぎます。 パッドを約1分間浸してから、パッドを取り外して別の容器に入れます。 温度計の端をパッドの中央に挿入し、約5分間観察します。 温度の読み取り値が上昇し、透明なガラスを使用すると、容器の側面に曇りが見られる場合があります。 鋼繊維が錆の層で覆われると、最終的に温度の上昇が止まり、それがさらなる酸化を阻止します。
何が起こった? 酢の酢酸がスチールウールパッドの繊維のコーティングを溶かし、下のスチールを大気にさらしました。 保護されていない鋼の鉄は、酸素と結合してより多くの酸化鉄を生成し、その過程で熱を放出しました。 パッドを再び酢に浸し、乾燥した容器に戻すと、同じ温度上昇が見られます。 パッド内のすべての鉄が錆びるまで、この実験を何度も繰り返すことができますが、これにはおそらく数日かかります。