Bien qu'il s'agisse d'une simple composante de tout cours de chimie de base, les formules chimiques fournissent des informations vitales sur les ions et les composés, et les indices sont tout aussi importants que les éléments eux-mêmes. Par exemple, l'indice et ce qu'il représente est ce qui distingue le gaz toxique monoxyde de carbone (CO) du dioxyde de carbone (CO2), un gaz formé dans la respiration humaine et consommé dans la photosynthèse.
TL; DR (trop long; n'a pas lu)
Les nombres en indice vous indiquent combien de chaque élément, groupe chimique ou ion sont présents dans une molécule.
Formules chimiques
Les formules chimiques utilisent des lettres et des chiffres pour représenter des espèces chimiques (c'est-à-dire des composés, des ions).
Les lettres proviennent du tableau périodique et représentent des éléments présents dans l'espèce. Un élément peut être représenté par une lettre majuscule, ou une lettre majuscule et une lettre minuscule. (Dans de rares cas, une lettre majuscule et deux lettres minuscules peuvent être utilisées.) La lettre ou les lettres qui représentent un élément sont appelées son symbole atomique.
Les nombres apparaissant en indices dans la formule chimique indiquent le nombre d'atomes de l'élément immédiatement avant l'indice. Si aucun indice n'apparaît, un atome de cet élément est présent.
Structure chimique
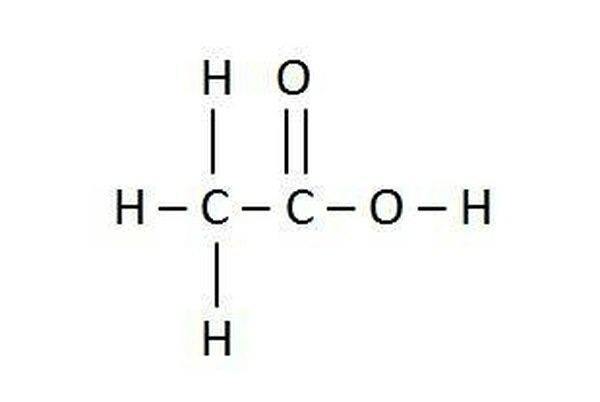
Les indices dans les formules chimiques peuvent également indiquer la structure des espèces, en particulier les espèces organiques.
Notez la molécule organique d'acide acétique donnée dans l'image. La formule chimique C2H4O2 est correcte, mais la formule CH3COOH donne aux chimistes une image plus claire de la molécule.
Indices et parenthèses
Parfois, les chimistes veulent reconnaître rapidement des ions ou des espèces chimiques présentes dans un composé. Lorsqu'une telle espèce apparaît plus d'une fois dans un composé, il est courant de mettre l'espèce entre parenthèses. L'indice qui suit immédiatement la parenthèse finale indique combien de fois cette espèce apparaît dans le composé.
Par exemple, la formule Ca (NO3)2 indique que deux NON3- des ions (nitrates) sont présents dans le composé Ca (NO3)2.
Stoechiométrie
La stoechiométrie est le processus d'équilibrage des équations chimiques, et les indices dans les formules chimiques jouent un rôle important. Les élèves en chimie utilisent des indices pour calculer le nombre de moles (une mesure de la quantité d'une substance) de chaque élément de chaque côté de l'équation.
Il est important de se rappeler que chaque indice est une partie immuable de l'identité d'un composé. Lors de l'équilibrage des équations, seuls les coefficients (les nombres devant les composés dans une équation chimique) sont modifiés, pas les indices.
Polymères
Un polymère est un grand composé dans lequel un groupe d'éléments apparaît plusieurs fois de suite. Ce groupe d'éléments est appelé un monomère. Dans une formule chimique, les monomères apparaissent entre parenthèses, tout comme les ions, uniquement au milieu de la formule. L'indice appartenant à un monomère n'a pas besoin d'être un nombre; ça peut être une variable.
Par exemple, un monomère dans le polypropylène peut être représenté par (CH2CHCH3) n.
