Kulstof er et ikke-metallisk element med et kemisk symbol på C. Det er det fjerde mest udbredte element i universet og det 15. mest udbredte element i jordskorpen. Det er også det næstmest forekommende element hos mennesker efter ilt. Dens kemiske sammensætning fører til flere unikke egenskaber af kulstof.
Kulstof hører til gruppe 14 i det periodiske system. Dens atomnummer er 6, og det har en atomvægt på 12.011. Oxidationstilstandene for kulstof kan variere fra -4 til +4, hvor +4 findes i forbindelser såsom methan og carbondisulfid og +2 for carbonmonoxid.
De fysiske egenskaber ved forskellige kulstofallotroper gør dem nyttige i batterier, elektronik og nanomaterialer. Kulstof er også ”kongen af grundstoffer”, som næsten danner 10 millioner forbindelser til dato inklusive organiske, uorganiske og organometalliske forbindelser.
Isotoper af kulstof anvendes i vid udstrækning til datering af radiocarbon (kulstof-14), molekylær struktur og medicinsk forskning (kulstof-13). Derudover udviser kulfibre fremragende mekaniske egenskaber og er populære inden for rumfart og anlæg.
Allotropes af kulstof
Kulstof har forskellige allotropiske formermed forskellige molekylære konfigurationer og atomstrukturer. De fysiske egenskaber ved kulstof varierer meget med hver allotrop. Nogle af de mest kendte allotrope af kulstof inkluderer grafit, diamant og fullerener.
Grafit er et af de blødeste kendte materialer og bruges i blyanter og som et fast smøremiddel. Det er også en god leder af elektricitet, hvilket gør det nyttigt i batterier og solpaneler.
Grafen er simpelthen et atomlag af grafit arrangeret i et bikagegitter. I et grafenlag er hvert carbonatom bundet kovalent til tre andre atomer, hvilket efterlader den fjerde elektron fri til at migrere i planet, dermed dets elektriske ledningsevne.
Tværtimod er diamant det hårdeste naturligt forekommende stof og er en af kulstofens unikke egenskaber. Det har næsten det dobbelte af densiteten af grafit, og hvert carbonatom er bundet tetraedrisk til fire andre uden fritflydende elektroner. Således er diamant en dårlig leder af elektricitet. Diamant er også klar i udseende, i modsætning til grafit, som er uigennemsigtig.
Forskere har også syntetiseret andre allotroper af kulstof, såsom fullerener, carbon nanofoams og andre. De besidder særlige egenskaber og udgør et blomstrende forskningsområde i nanomaterialer. Fullerener er en gruppe af hule kulmolekyler i et lukket bur (buckyball) eller cylinder (carbon nanorør) konformation.
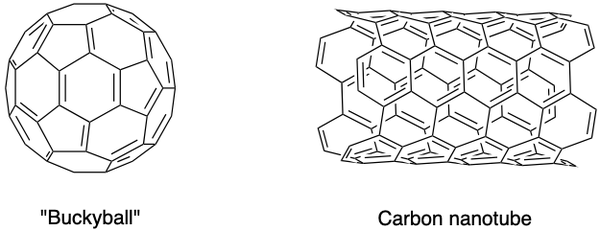
•••Oprettet ved hjælp af ChemDraw
C60 buckyball blev opdaget af Sir Harold Kroto, Richard Smalley og Robert Curl Jr. ved hjælp af en laser til at fordampe grafitstænger i en heliumatmosfære. Kulstofatomerne er forbundet med enkelt- og dobbeltbindinger for at danne 12 femkantede og 20 sekskantede flader i en fodboldboldform. Deres banebrydende indsats gav dem Nobelprisen i 1996.
Carbon nanorør, som er aflange versioner af buckyballs, blev identificeret af Iijima Sumio. De er fremragende ledere af varme og elektricitet og er nyttige til elektronik.
Carbon-nanorør udviser også imponerende trækstyrke og har spændende anvendelser inden for strukturmaterialer og medicin. Imidlertid har den kontrollerede syntese af sådanne nanomaterialer udgjort en stor udfordring for forskere.
Kemisk reaktivitet af kulstof
Kulstof danner grundlaget for livet på Jorden, hvor millioner af kulstofholdige forbindelser udgør 18 procent af alle levende ting. Det kan danne stabile, kovalente bindinger med andre atomer og fremstå som lange kæder eller ringe med stærke sammenkoblede kulstof-kulstofbindinger. Disse bidrager til mangfoldigheden og kompleksiteten af kulstofforbindelser, der findes på Jorden.
Disse kulstofforbindelser inkluderer organiske molekyler, såsom proteiner, kulhydrater og DNA, der findes i cellerne i levende organismer såvel som uorganiske forbindelser som carbonoxider. Undersøgelsen af organiske molekyler udgør et specialiseret felt kaldet organisk kemi. Kulstof kan også danne kovalente bindinger med metal som organometalliske forbindelser. Jernporphyrin, som er iltbindingsstedet for hæmoglobin, er et sådant eksempel.
På trods af sin overflod i naturen er kulstof relativt reaktivt under normale forhold. Ved standard temperatur er den ikke reaktiv over for syrer (svovlsyre eller saltsyre) eller baser. Det er også stabilt over for oxidation ved denne temperatur. Ved højere temperaturer kan imidlertid kulstof reagere med ilt til dannelse af carbonoxider (CO2 og CO) med svovlgas til dannelse af carbondisulfid og med silicium til dannelse af carbider.
Isotoper af kulstof
Der er 15 kendte isotoper af kulstof, hvoraf kulstof-12 (98,93 procent naturligt kulstof) og kulstof-13 (1,07 procent) er de to stabile isotoper. Carbon-14 er den længstlevede isotop med en halveringstid på 5.730 år. Den kortvarige kulstofisotop er kulstof-8, og den har en halveringstid på 1,98739 x 10−21 sekunder.
Isotopen carbon-14 er repræsenteret af 146C, hvor presuperscript 14 er atommassen, og presubscript 6 er atomnummeret. Carbon-14 har en meget lav naturlig overflod (0,00000001 procent), men dens lange halveringstid gør den nyttig til radiometrisk dating.
Carbon-14 dannes, når nitrogen-14 reagerer med neutroner fra kosmisk stråling og frigiver en proton i denne proces. Carbon-14 reagerer derefter med ilt til dannelse 14CO2, som er jævnt fordelt i atmosfæren med 12CO2.
147N + 10n> 146C + 11s
Kulstofcyklussen starter, når levende organismer omdanner kuldioxid (14CO2 og 12CO2 fra atmosfæren) til organiske forbindelser ved fotosyntese og frigive det tilbage til atmosfæren ved åndedræt. I denne ligevægt er der et fast forhold på 14CO2 og 12CO2 i organismerne. Men når de dør, stopper ligevægten, og kulstof-14 gennemgår beta-forfald til nitrogen-14 i henhold til dets 5.730 års halveringstid.
146C> 147N + 0-1e
Måling af den relative andel af kulstof-14 i en død prøve tillader således beregning af den forløbne tid efter dens død. Denne metode til datering af radiocarbon er blevet brugt i vid udstrækning til datering af fossiler og arkæologiske prøver fra 500 til 50.000 år gamle.
Carbon-13 er en anden isotop, der bruges i vid udstrækning i mange applikationer. For eksempel bruges det i kernemagnetisk resonans (NMR) til bestemmelse af molekylære strukturer af organiske forbindelser. Det bruges også som et mærkningsværktøj i kombination med et massespektrometer til medicinsk forskning.
Mekaniske egenskaber ved kulfibre
Kulstof udviser også nyttige mekaniske egenskaber, bortset fra dets fysiske, kemiske og nukleare egenskaber.
Det kan danne sig legeringer med stål til kulstofstål, hvoraf kulstofindholdet varierer fra 0,05 til 2 vægtprocent. Medium kulstofstål (0,3-0,6 procent kulstof) har afbalanceret styrke og duktilitet samt fremragende trækstyrke. Gennem en varmebehandlingsproces kan ultrahøjt kulstofstål (1,25-2 procent kulstof) hærdes til stor hårdhed og anvendes til fremstilling af knive.
Kulfibre, der er 5 til 10 um tykke fibre, der hovedsageligt består af kulstofatomer, viser høje stivhed, trækstyrke, kemisk resistens, temperaturtolerance og lav vægt og termisk udvidelse. Fladstyrken for stål afhænger af dets kvalitet, og blødt stål har en flydespænding på 247 MPa. Kulfibre har trækstyrker fra 1.600 til 6.370 MPa og er derfor populære inden for luftfart, anlæg og sport.
Når en belastning udøves på et materiale, deformeres det først elastisk. På dette tidspunkt kan den vende tilbage til sin oprindelige form, når spændingen fjernes. Udbytte styrke er defineret som den belastning et materiale kan modstå uden permanent deformation.
Når det når et punkt (øvre flydepunkt), hvor det ikke længere kan vende tilbage til dets oprindelige dimensioner, gennemgår det plastisk deformation, hvilket er en permanent og irreversibel. Trækstyrke er den maksimale styrke, som et materiale kan modstå uden at mislykkes eller brydes.
