Du har antagligen stött på att batterierna går ur, vilket är en olägenhet om du försöker använda dem i elektroniska enheter. Cellkemi i batterier kan berätta egenskaperna för hur de fungerar inklusive hur de går platta.
Cellkemi av batterier
•••Syed Hussain Ather
När den elektrokemiska reaktionen hos ett batteri tömmer materialet går batteriet urladdat. Detta händer vanligtvis efter en lång tid med batterianvändning.
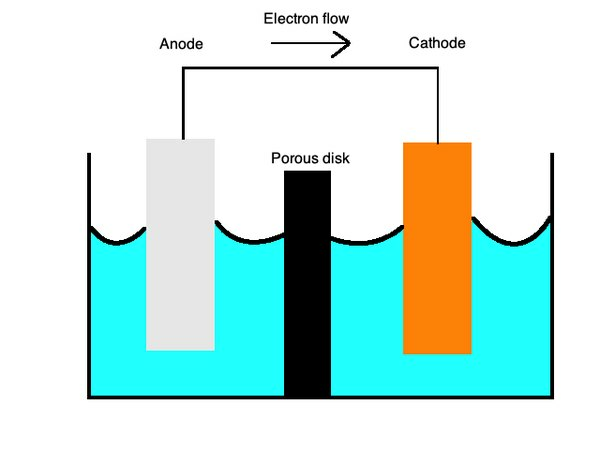
Batterier använder i allmänhet primära celler, en typ avgalvanisk cellsom använder två olika metaller i en flytande elektrolyt för att möjliggöra överföring av laddning mellan dem. Positiva laddningar strömmar frånkatod, byggd med katjoner eller positivt laddade joner som koppar, tillanod, med anjoner eller negativt laddade joner såsom zink.
Tips
Batterierna går tomma som ett resultat av att elektrolytens kemikalier torkar in i batteriet. När det gäller alkaliska batterier är detta när all mangandioxid har omvandlats. I detta skede är batteriet urladdat.
För att komma ihåg detta förhållande kan du komma ihåg ordet "OILRIG." Detta säger dig det
Primära celler kan också arbeta med enskilda halvceller av olika metaller i en jonlösning förbunden med en saltbrygga eller ett poröst membran. Dessa celler ger batterier en mängd användningsområden.
Alkaliska batterier, som specifikt använder reaktionen mellan en zinkanod och en magnesiumkatod, används för ficklampor, bärbara elektroniska enheter och fjärrkontroller. Andra exempel på populära batterielement inkluderar litium, kvicksilver, kisel, silveroxid, kromsyra och kol.
Tekniska konstruktioner kan dra nytta av hur batterierna går tomma för att spara och återanvända energi. Billiga hushållsbatterier använder i allmänhet kol-zinkceller som är utformade så att om zinken genomgårGalvanisk korrosion, en process där en metall korroderar företrädesvis, kan batteriet producera elektricitet som en del av en sluten elektronkrets.
Vid vilken temperatur exploderar batterier? Cellkemi för litiumjonbatterier innebär att dessa batterier startar kemiska reaktioner som resulterar i deras explosion vid cirka 1000 ° C. Kopparmaterialet inuti dem smälter vilket gör att de inre kärnorna går sönder.
Den kemiska cellens historia
1836 konstruerade den brittiska kemisten John Frederic DaniellDaniell celldär han använde två elektrolyter, istället för bara en, för att låta väte som produceras av den ena konsumeras av den andra. Han använde zinksulfat istället för svavelsyra, en vanlig praxis för tidens batterier.
Innan dess använde forskare voltaiska celler, en typ av kemisk cell som använder en spontan reaktion, som förlorade kraft i snabba hastigheter. Daniell använde en barriär mellan koppar- och zinkplattorna för att förhindra att överflödigt väte bubblade och förhindra att batteriet snabbt slits ut. Hans arbete skulle leda till innovationer inom telegrafi och elektrometallurgi, metoden att använda elektrisk energi för att producera metaller.
Hur laddningsbara batterier går ur
Sekundära cellerå andra sidan är uppladdningsbara. Det uppladdningsbara batteriet, även kallat lagringsbatteri, sekundärcell eller ackumulator, lagrar laddning över tiden när katoden och anoden är anslutna i en krets med varandra.
Vid laddning oxideras den positiva aktiva metallen, såsom nickeloxidhydroxid, vilket skapar elektroner och förlora dem, medan det negativa materialet som kadmium reduceras, fånga elektroner och vinna dem. Batteriet använder laddningsurladdningscykler med olika källor, inklusive växelström som en extern spänningskälla.
Uppladdningsbara batterier kan fortfarande bli tomma efter upprepad användning eftersom materialet som är involverat i reaktionen tappar sin förmåga att ladda och ladda om. När dessa batterisystem slits ut finns det olika sätt att batterierna går ur.
Eftersom batterier används rutinmässigt kan vissa av dem, såsom blybatterier, tappa förmågan att ladda. Litium av litiumjonbatterier kan bli reaktiva litiummetaller som inte kan återgå till laddningsurladdningscykeln. Batterier med flytande elektrolyter kan minska i fukt på grund av avdunstning eller överladdning.
Användning av uppladdningsbara batterier
Dessa batterier används vanligtvis i bilstartare, rullstolar, elektriska cyklar, elverktyg och batterilagringskraftverk. Forskare och ingenjörer har studerat deras användning i hybridförbränningsbatterier och elfordon för att bli mer effektiva i sin energianvändning och hålla längre.
Det uppladdningsbara blybatteriet bryter vattenmolekyler (H2Oi vattenhaltig vätelösning (H+) och oxidjoner (O2-) som producerar elektrisk energi från den trasiga bindningen när vattnet tappar sin laddning. När den vattenhaltiga vätelösningen reagerar med dessa oxidjoner används de starka O-H-bindningarna för att driva batteriet.
Fysik av batterireaktioner
Denna kemiska energi driver en redoxreaktion som omvandlar högenergireaktanter till produkter med lägre energi. Skillnaden mellan reaktanterna och produkterna låter reaktionen ske och bildar en elektrisk krets när batteriet kopplas upp genom att omvandla kemisk energi till elektrisk energi.
I en galvanisk cell har reaktanterna, såsom metalliskt zink, en hög fri energi som låter reaktionen ske spontant utan yttre kraft.
Metallerna som används i anoden och katoden har gitter sammanhängande energier som kan driva den kemiska reaktionen. Gitterens sammanhängande energi är den energi som krävs för att separera atomerna som gör metallen från varandra. Metalliskt zink, kadmium, litium och natrium används ofta eftersom de har höga joniseringsenergier, den minsta energi som krävs för att avlägsna elektroner från ett element.
Galvaniska celler som drivs av joner av samma metall kan använda skillnader i fri energi för att få Gibbs fri energi att driva reaktionen. DeGibbs fri energiär en annan form av energi som används för att beräkna mängden arbete en termodynamisk process använder.
I det här fallet är förändringen i standard Gibbs fri energiGo driver spänningen eller elektromotorisk kraftEoi volt, enligt ekvationen
E ^ {\ text {o}} = \ frac {- \ Delta_rG ^ {\ text {o}}} {v_eF}
i vilkenveär antalet elektroner som överförs under reaktionen och F är Faradays konstant (F = 96485,33 C mol−1).
DeΔrGo indikerar att ekvationen använder förändringen i Gibbs fri energi (ΔrGo =Gslutlig - Gförsta).Entropi ökar när reaktionen använder den tillgängliga fria energin. I Daniell-cellen står den sammanhängande energidifferensen mellan zink och koppar för de flesta av Gibbs fria energidifferenser när reaktionen inträffar.ΔrGo= -213 kJ / mol, vilket är skillnaden i Gibbs fri energi för produkterna och för reaktanterna.
Spänning av en galvanisk cell
Om du separerar den elektrokemiska reaktionen i en galvanisk cell i halva reaktionerna av oxidation och reduktion processer kan du summera motsvarande elektromotoriska krafter för att erhålla den totala spänningsskillnaden som används i cell.
Till exempel kan en typisk galvanisk cell använda CuSO4 och ZnSO4 med standard potentiella halvreaktioner som:Cu2+ + 2 e− ⇌ Cumed motsvarande elektromotorisk potentialEo = +0,34 VochZn2+ + 2 e− ⇌ Znmed potentialEo = −0,76 V.
För den övergripande reaktionen,Cu2+ + Zn ⇌ Cu + Zn2+ , kan du "vända" halvreaktionsekvationen för zink medan du vänder tecknet på den elektromotoriska kraften för att erhållaZn ⇌ Zn2+ + 2 e− medEo = 0,76 V.Den totala reaktionspotentialen, summan av de elektromotoriska krafterna, är då+0,34 V. - (−0,76 V) = 1,10 V.
