Chemický vzorec je zjednodušený štandardný zápis na vysvetlenie chemickej reakcie použitej v experimentoch. Možno vyzerajú komplikovane, ale keď sa naučíte, ako ich čítať, stanú sa dosť vysvetliteľnými.
Pozerajte sa na chemickú reakciu, ktorú sa pokúšate rozložiť, ako na rovnicu. Hľadajte kľúčové slová, konkrétne príslušné chemické zložky. Napríklad metán (CH4) sa spaľuje, čo vždy znamená, že sa to deje v kyslíku (O2). Takto sa získa oxid uhličitý (CO2) a vodná para (H2O). Poznačte si umiestnenie slova „Výnosy“, pretože je to dôležité.
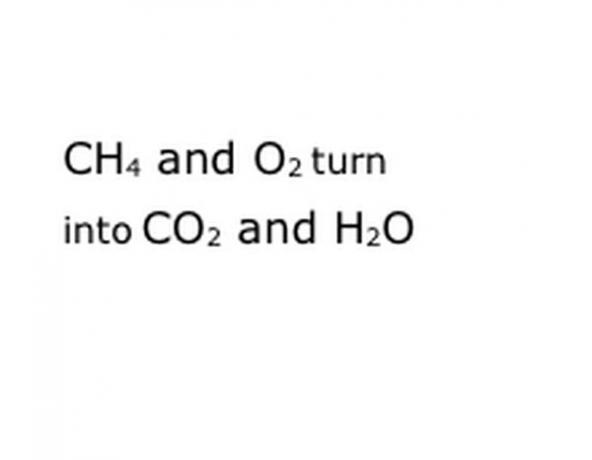
Chemické zložky reakcie napíšte do štandardného formátu zápisu. V našom príklade to bude CH4, O2, CO2 a H2O. V chémii znamená „výťažok“ to, že čokoľvek je predtým, sa zmení na to, čo príde potom, takže buďte istí, že „výťažok“ je zhruba v strede. Táto fráza bude predstavovať skutočnú chemickú reakciu, v tomto prípade horenie. Takže všetko, čo spálite, musí byť pred tým a všetko, po čom musí byť reakcia, musí byť.
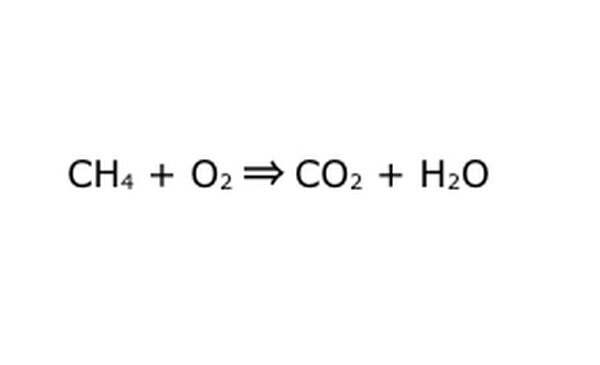
Opíšte rovnicu ako matematický proces. Výrazy „výťažok“ alebo „premena na“ nahraďte šípkou a medzi chemické zložky nakreslite znamienka plus. Pre zjednodušenie si každú chemickú zložku predstavte ako samostatnú molekulu. Môže to pomôcť nakresliť molekuly na kúsku papiera. Zaistite, aby všetky molekuly, ktoré vstupujú, boli zastúpené tak, že vystupujú. Ak v konečnom produkte niečo chýba, môžete to pridať spôsobom, ktorý dáva zmysel - porovnajte čokoľvek s tým, čo viete o kovalentnom spájaní. Pretože väčšina experimentov sa deje v normálnej atmosfére, môžete do horiacich reakcií pridať prípadne O2. Ak je rovnica reverzibilná, uistite sa, že má dvojitú šípku, ktorá to predstavuje.
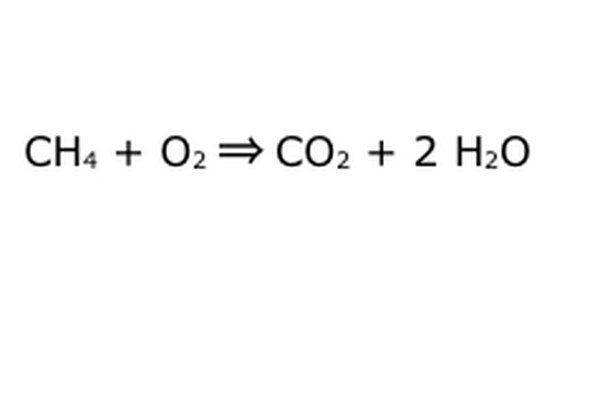
Vyvážte svoju rovnicu. Tu vstupuje do hry zákon zachovania: myslite na šíp, našu reakciu, ako na stroj, do ktorého ste vyhodili všetky komponenty naľavo. Stroj nebude vyrábať ani pridávať nič, čo ste nevložili, a preto vypľuje iba to isté množstvo vecí, ktoré ste vložili. V tomto presnom okamihu máme okolo dve prebytočné molekuly vodíka, pretože ste vložili „4“. Jediné miesto, kde môže v tomto stroji ísť, je jeden z produktov, takže bude musieť prejsť do molekúl vody. Napíš „2“ pred H2O, čo znamená, že za každý vložený CH4 dostaneš späť dve H2O.

Upozorňujeme, že s našou rovnicou stále existuje malý problém: dovnútra nie je dostatok kyslíka. Vychádzajú štyri atómy kyslíka, ale vstupujú do nich iba dva, a tak je to celé stále nevyvážené. Napíšte „2“ pred O2, aby ste vyjadrili, že musíte vložiť dva O2, aby ste mali dostatok reakcie.
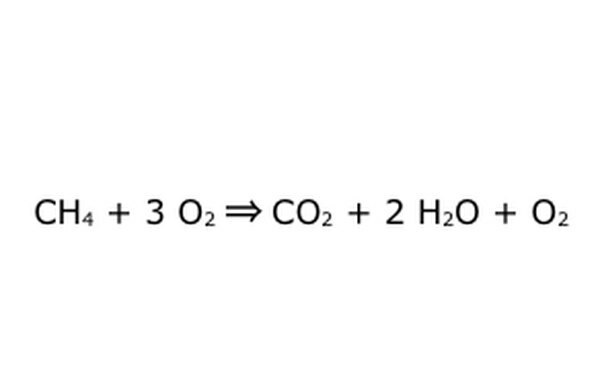
Všimnite si, že je možné taký proces urobiť „v prebytku kyslíka“. To znamená, že rovnica vloží viac kyslíka, ako je potrebné, a dostane späť. Napríklad si všimnite, že do nej vstupuje ďalšie O2, takže prichádza ďalšie. Len sa uistite, že zákon zachovania je vždy dodržiavaný. Všetko, čo vojde, musí vyjsť.
Tipy
Všeobecne sa chemikálie v týchto typoch rovníc merajú v moloch. Krt je jednotka, ktorá predstavuje 6,0221415 10 ^ (23) molekúl. Pretože je to príliš veľké číslo na to, aby sme ho pochopili, je ľahšie pri rovnováhe myslieť na jednotlivé molekuly. Uvedomte si to pri štartovaní.
