Destilacija je metoda za odvajanje komponenata od tekuće smjese, iskorištavanjem njihovih razlika u vrelištima. Odvajanje je tekućina-plin i uključuje isparavanje i naknadnu kondenzaciju svake tekućine. Neke su prednosti frakcijske destilacije u odnosu na jednostavnu destilaciju.
Uobičajene vrste destilacije su jednostavna destilacija, frakcijska destilacija, vakuumska destilacija i destilacija vodenom parom. Razlikuju se uglavnom u postavljanju uređaja i njihovoj primjeni.
Frakcijska destilacija učinkovitija je od jednostavne destilacije u odvajanju zbog velikog broja teorijskih ploča. To je važan proces u kemiji, industriji i prehrambenoj znanosti. Upotreba frakcijske destilacije uključuje procese poput desalinizacije, rafiniranja sirove nafte i kemijskog pročišćavanja.
Vrste destilacije
Jednostavna destilacija učinkovita je samo za tekućine čija se vrelišta razlikuju za više od 30 ° C. Suprotno tome, frakcijska destilacija prikladna je za zahtjevnija odvajanja, gdje je razlika u vrelištu manja od 30 ° C.
Teorija frakcijske destilacije
Treba razumjeti kako funkcionira frakcijska destilacija Raoultov zakon, koji navodi da tlak pare otopine ovisi o tlaku pare svake komponente i molskom udjelu komponente u otopini. Držeći tlak konstantnim, može se stvoriti a dijagram temperature i sastava.
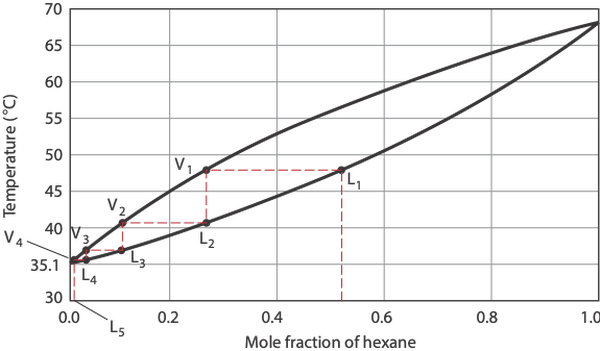
•••Izmijenjeno iz Laboratorijske tehnike u organskoj kemiji (četvrto izdanje, 2014): stranice 173-206
Za smjesu pentan-heksana pri jednom atmosferskom tlaku, početna tekuća smjesa (L1) heksana (bp = 69 ° C) i pentana (bp = 36 ° C) vreli na 48 ° C da bi se stvorila para V1, koji se kondenzira u oblik L2. Nakon prvog ciklusa isparavanja i kondenzacije, postotak pentana povećao se s 48 na 73 posto.
L2 zatim isparava u V2, što rezultira daljnjim obogaćivanjem pentanom. L5, koji je tekućina dobivena nakon četiri ciklusa, gotovo je čisti pentan. Svaki ciklus isparavanja-kondenzacije, također nazvan teorijska ploča, daje čistiju otopinu hlapljivije komponente.
Prednosti frakcijske destilacije u odnosu na jednostavnu destilaciju
U uređaju za frakcijsku destilaciju, frakcionirajuća kolona se obično postavlja između tikvice za destilaciju i glave kako bi se povećalo odvajanje tekućina od smjese. Ti stupovi imaju veću površinu na kojoj mogu nastati ravnoteže tekuće pare i time više teoretskih ploča. Primjeri frakcionirajućih stupova su stupovi Vigreux i staklene kuglice koji imaju šest do osam teorijskih ploča.
Pri jednostavnoj destilaciji ne koristi se frakcionirajuća kolona, a para iz tikvice za destilaciju ide ravno u kondenzaciju. Ima samo jednu ili dvije teoretske ploče, pa ne bi bio učinkovit za odvajanje smjesa poput L1, koji za pročišćavanje zahtijeva više od četiri ciklusa isparavanja-kondenzacije.
Primjene frakcijske destilacije
Frakcijska destilacija koristi se u rafinerije nafte za razdvajanje sirove nafte u ugljikovodike koji imaju različit broj ugljika, vrelišta i primjenu. Neki od izoliranih proizvoda uključuju benzin, dizel, ulja i voskove. Ova se metoda također koristi u kemijskim postrojenjima, postrojenjima za preradu prirodnog plina i kriogenim odvajanjem zraka.
Frakcijska destilacija je također a uobičajena tehnika u laboratorijima organske kemije. Na primjer, ciklopentadien se obično prodaje kao diciklopentadien, jer se ciklopentadien može spontano dimerizirati da bi nastao diciklopentadien. Frakcijska destilacija često se koristi za vraćanje diciklopentadiena natrag u ciklopentadien.
Utjecaj frakcijske destilacije na okoliš
Frakcijska destilacija sama po sebi nije štetna za okoliš. Zapravo se frakcijskom destilacijom sirova nafta, inače neupotrebljiva, pretvara u vrijednije proizvode. Međutim, naftne rafinerije, u kojima se vrši frakcijska destilacija sirove nafte, mogu biti izvor onečišćenja ako se sa nusproizvodima ne postupa na odgovarajući način u skladu s propisima.
Rafinerije su glavni izvor onečišćivača zraka kao što su čestice, dušični oksidi i ugljični monoksid. Otpadne vode iz rafinerija također uzrokuju onečišćenje vode i zemljišta jer se talože u vodonosnicima, tlu i podzemnim vodama.
