Destillatie is een methode om componenten uit een vloeibaar mengsel te scheiden door gebruik te maken van hun kookpuntverschillen. Het is een vloeistof-gasscheiding en omvat de verdamping en daaropvolgende condensatie van elke vloeistof. Er zijn enkele voordelen van gefractioneerde destillatie ten opzichte van eenvoudige destillatie.
Veel voorkomende soorten destillatie zijn eenvoudige destillatie, gefractioneerde destillatie, vacuümdestillatie en stoomdestillatie. Ze verschillen voornamelijk in de opstelling van het apparaat en hun toepassingen.
Gefractioneerde destillatie is efficiënter dan eenvoudige destillatie bij scheiding vanwege een groot aantal theoretische platen. Het is een belangrijk proces in de chemie, industrie en voedingswetenschap. Gebruik van gefractioneerde destillatie omvat processen zoals ontzilting, raffinage van ruwe olie en chemische zuivering.
Soorten distillatie
Eenvoudige distillatie is alleen effectief voor vloeistoffen waarvan het kookpunt meer dan 30 °C verschilt. Integendeel, gefractioneerde destillatie is geschikt voor meer uitdagende scheidingen, waarbij het kookpuntverschil minder dan 30 °C is.
Theorie van fractionele destillatie
Om te begrijpen hoe fractionele destillatie werkt, moet men weten: Wet van Raoult, waarin staat dat de dampdruk van een oplossing afhankelijk is van de dampdruk van elke component en de molfractie van de component in de oplossing. Terwijl de druk constant wordt gehouden, kan men een temperatuur-samenstellingsdiagram.
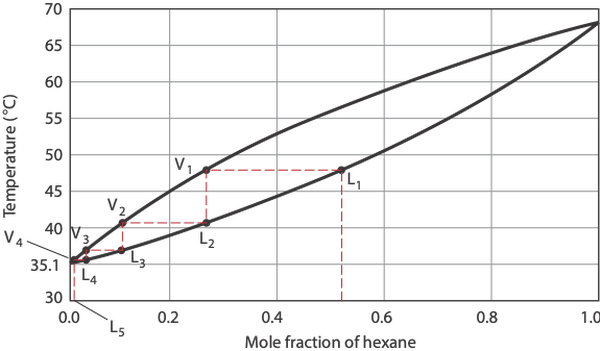
•••Aangepast van Laboratory Technique in Organic Chemistry (vierde editie, 2014): pagina's 173-206
Voor een pentaan-hexaanmengsel bij één atmosferische druk, een aanvankelijk vloeibaar mengsel (L1) hexaan (bp = 69°C) en pentaan (bp = 36°C) kookt bij 48°C om damp V te produceren1, die condenseert tot L2. Na de eerste verdampings-condensatiecyclus is het percentage pentaan gestegen van 48 procent naar 73 procent.
L2 verdampt vervolgens in V2, wat resulteert in een verdere verrijking in pentaan. L5, de vloeistof die na vier cycli wordt verkregen, is bijna puur pentaan. Elke verdampings-condensatiecyclus, ook wel theoretische plaat, levert een zuiverdere oplossing van de meer vluchtige component op.
Voordelen van fractionele destillatie ten opzichte van eenvoudige destillatie
In een gefractioneerde destillatieopstelling wordt typisch een fractioneringskolom tussen de destillatiekolf en de kop geplaatst om de scheiding van vloeistoffen uit het mengsel te vergroten. Deze kolommen hebben een groter oppervlak waarop vloeistof-dampevenwichten kunnen optreden en dus meer theoretische platen. Voorbeelden van fractioneringskolommen zijn Vigreux- en glasparelskolommen, die zes tot acht theoretische platen hebben.
Bij een eenvoudige destillatie wordt geen fractioneerkolom gebruikt en gaat damp uit de destillatiekolf rechtstreeks in condensatie. Het heeft slechts een of twee theoretische platen, dus het zou niet effectief zijn voor de scheiding van mengsels zoals L1, waarvoor meer dan vier verdampings-condensatiecycli nodig zijn om te zuiveren.
Gebruik van fractionele destillatie
Fractionele destillatie wordt gebruikt in olieraffinaderijen om ruwe olie te scheiden in koolwaterstoffen, die verschillende koolstofgetallen, kookpunten en toepassingen hebben. Enkele van de geïsoleerde producten zijn benzine, diesel, oliën en wassen. Deze methode wordt ook gebruikt in chemische fabrieken, aardgasverwerkingsinstallaties en cryogene luchtscheidingsinstallaties.
Fractionele distillatie is ook een veelgebruikte techniek in laboratoria voor organische chemie. Cyclopentadieen wordt bijvoorbeeld gewoonlijk verkocht als dicyclopentadieen omdat cyclopentadieen spontaan kan dimeriseren om dicyclopentadieen te vormen. Gefractioneerde destillatie wordt vaak gebruikt om dicyclopentadieen weer om te zetten in cyclopentadieen.
Milieu-impact van fractionele destillatie
Fractionele distillatie alleen is niet schadelijk voor het milieu. In feite zet gefractioneerde destillatie ruwe olie, die anders onbruikbaar zou zijn, om in waardevollere producten. Aardolieraffinaderijen, waar gefractioneerde destillatie van ruwe olie wordt uitgevoerd, kunnen echter een bron van vervuiling zijn als de bijproducten niet goed volgens de voorschriften worden behandeld.
Raffinaderijen zijn een belangrijke bron van luchtverontreinigende stoffen zoals fijnstof, stikstofoxiden en koolmonoxide. Afvalwater van de raffinaderijen veroorzaakt ook water- en landvervuiling omdat het bezinkt in watervoerende lagen, bodem en grondwater.
