Rumus kimia adalah notasi standar yang disederhanakan untuk menjelaskan reaksi kimia yang digunakan dalam eksperimen. Mereka mungkin terlihat rumit, tetapi ketika Anda belajar cara membacanya, mereka menjadi cukup jelas.
Lihatlah reaksi kimia yang Anda coba pecahkan sebagai persamaan. Cari kata kunci, khususnya komponen kimia yang terlibat. Misalnya, metana (CH4) dibakar, yang berarti selalu dilakukan dengan oksigen (O2). Ini menghasilkan uap karbon dioksida (CO2) dan air (H2O). Perhatikan lokasi kata "Hasil", karena ini penting.
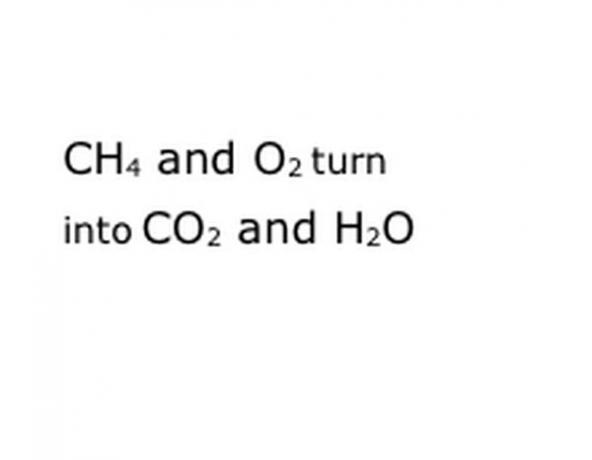
Tuliskan komponen kimia dari reaksi dalam format notasi standar. Dalam contoh kita, ini akan menjadi CH4, O2, CO2 dan H2O. Dalam kimia, "hasil" berarti bahwa apa pun yang sebelum berubah menjadi apa pun yang datang setelahnya, jadi pastikan bahwa "hasil" kira-kira berada di tengah. Ungkapan itu akan mewakili reaksi kimia yang sebenarnya, dalam hal ini pembakaran. Jadi apa pun yang akan Anda bakar harus sebelum itu, dan apa pun yang dihasilkan reaksi harus sesudahnya.
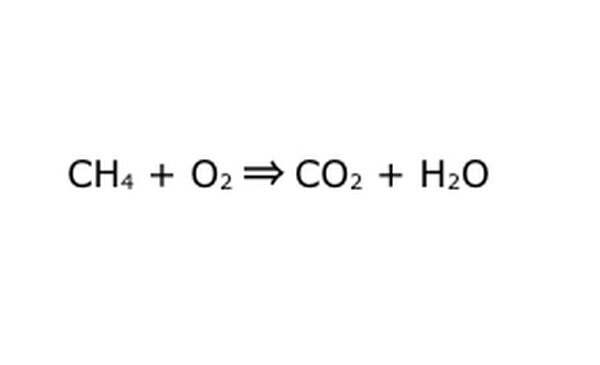
Tulis ulang persamaan tersebut sebagai proses matematika. Ganti "hasil" atau "berubah menjadi" dengan panah, dan gambar tanda plus di antara komponen kimianya. Untuk menyederhanakan, pikirkan setiap komponen kimia sebagai molekul individu. Mungkin membantu untuk menarik molekul keluar pada selembar kertas bekas. Pastikan semua molekul yang masuk terwakili keluar. Jika ada sesuatu yang hilang dari produk akhir, Anda dapat menambahkannya dengan cara yang masuk akal - periksa apa pun yang Anda ketahui tentang ikatan kovalen. Karena sebagian besar percobaan dilakukan di atmosfer biasa, Anda dapat menambahkan O2 jika perlu untuk reaksi pembakaran. Jika persamaannya reversibel, pastikan persamaan tersebut memiliki panah ganda untuk menyatakannya.
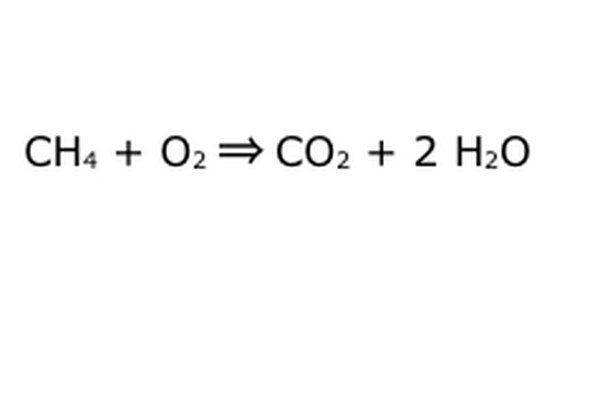
Seimbangkan persamaan Anda. Di sinilah Hukum Kekekalan berperan: pikirkan panah, reaksi kita, sebagai mesin tempat Anda membuang semua komponen di sebelah kiri. Mesin tidak akan membuat atau menambahkan apa pun yang tidak Anda masukkan, dan karena itu mesin hanya akan mengeluarkan jumlah barang yang sama dengan yang Anda masukkan. Pada saat yang tepat ini, kita memiliki dua molekul hidrogen berlebih yang mengambang, karena Anda memasukkan "4". Satu-satunya tempat yang bisa masuk ke mesin ini adalah ke salah satu produk, jadi itu harus masuk ke molekul air. Tulis "2" di depan H2O untuk menunjukkan bahwa untuk setiap CH4 yang Anda masukkan, Anda akan mendapatkan dua H2O kembali.

Perhatikan bahwa masih ada masalah kecil dengan persamaan kita: tidak ada cukup oksigen yang masuk. Ada empat atom oksigen yang keluar, tetapi hanya dua yang masuk, sehingga semuanya masih tidak seimbang. Tulis "2" di depan O2 untuk menyatakan bahwa Anda harus memasukkan dua O2 untuk mendapatkan reaksi yang cukup.
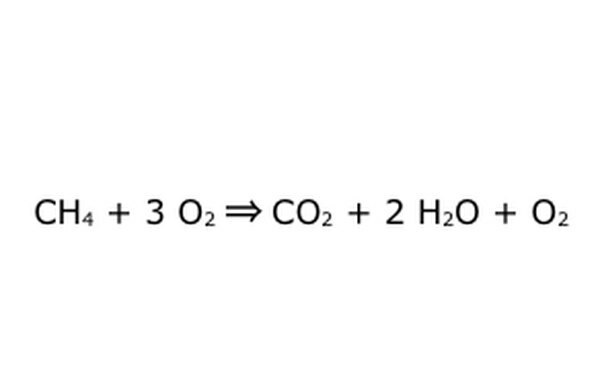
Perhatikan bahwa dimungkinkan untuk melakukan proses seperti ini "dengan oksigen berlebih". Apa artinya ini adalah persamaan memasukkan lebih banyak oksigen daripada yang dibutuhkan, dan mendapat lebih banyak kembali. Sebagai contoh, perhatikan bahwa ada tambahan O2 yang masuk, jadi ada tambahan yang keluar. Pastikan bahwa Hukum Konservasi dipatuhi setiap saat. Apa pun yang masuk harus keluar.
Tips
Umumnya, bahan kimia dalam jenis persamaan ini diukur dalam mol. Mol adalah satuan yang mewakili 6,0221415 10^(23) molekul. Karena ini adalah angka yang terlalu besar untuk dipahami, lebih mudah untuk berpikir dalam bentuk molekul tunggal ketika menyeimbangkan. Sadarilah hal ini saat memulai.
