화학 공식은 실험에 사용되는 화학 반응을 설명하기위한 단순화 된 표준 표기법입니다. 복잡해 보일 수 있지만 읽는 방법을 배우면 상당히 자명 해집니다.
분석하려는 화학 반응을 방정식으로보십시오. 키워드, 특히 관련된 화학 성분을 찾으십시오. 예를 들어, 메탄 (CH4)은 연소되어 항상 산소 (O2)에서 이루어집니다. 이것은 이산화탄소 (CO2)와 물 (H2O) 증기를 모두 생성합니다. 중요하므로 "Yields"라는 단어의 위치를 기록하십시오.
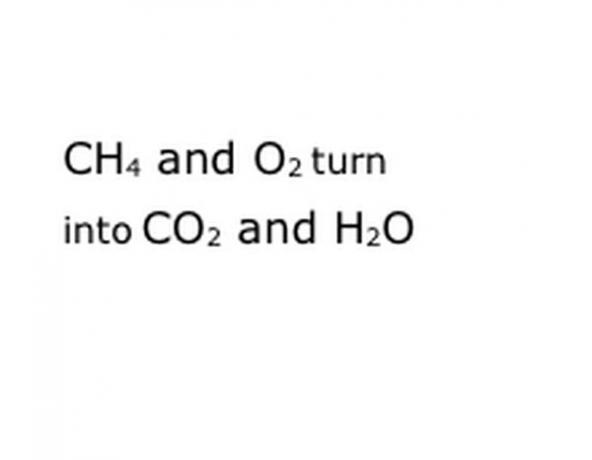
반응의 화학 성분을 표준 표기 형식으로 작성하십시오. 이 예에서는 CH4, O2, CO2 및 H2O가됩니다. 화학에서 "수율"은 이전에있는 것이 무엇이든 뒤에 오는 것으로 바뀌는 것을 의미하므로 "수율"이 대략 중간에 있어야합니다. 이 문구는 실제 화학 반응, 이 경우 연소를 나타냅니다. 따라서 당신이 태울 모든 것은 그 이전에 있어야하고, 반응이 산출되는 모든 것은 이후에 있어야합니다.
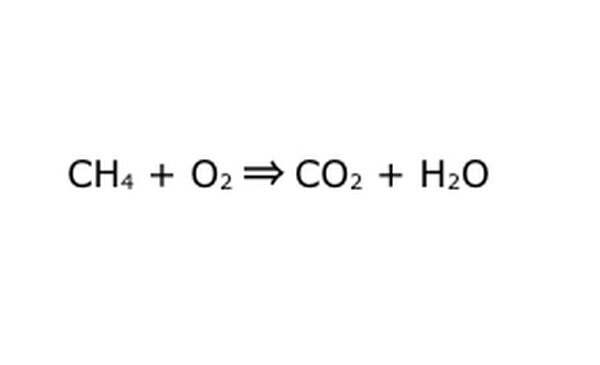
방정식을 수학적 과정으로 다시 작성하십시오. "yield"또는 "turns into"를 화살표로 바꾸고 화학 성분 사이에 더하기 기호를 그립니다. 일을 단순화하려면 각 화학 성분을 개별 분자로 생각하십시오. 스크랩 종이에 분자를 끌어내는 것이 도움이 될 수 있습니다. 들어가는 모든 분자가 나오는 것으로 표시되는지 확인하십시오. 최종 제품에서 누락 된 것이 있으면 의미있는 방식으로 추가 할 수 있습니다. 공유 결합에 대해 알고있는 내용과 비교하여 확인하십시오. 대부분의 실험은 일반 대기에서 이루어지기 때문에 필요한 경우 연소 반응에 O2를 추가 할 수 있습니다. 방정식이 가역적이면이를 나타내는 이중 화살표가 있는지 확인하십시오.
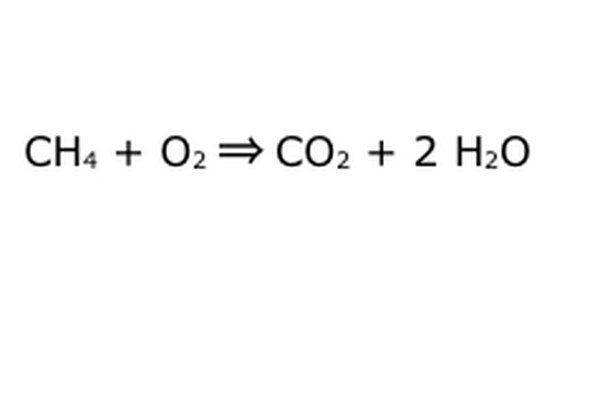
방정식의 균형을 유지하십시오. 이것이 바로 보존의 법칙이 작용하는 곳입니다. 화살표, 우리의 반응을 왼쪽의 모든 구성 요소를 버린 기계로 생각하십시오. 기계는 당신이 넣지 않은 것을 만들거나 추가하지 않기 때문에 당신이 넣은 것과 같은 양의 물건 만 뱉어 낼 것입니다. 이 정확한 순간에 우리는 "4"를 넣었 기 때문에 두 개의 과잉 수소 분자가 주위에 떠 있습니다. 이 기계에 들어갈 수있는 유일한 장소는 제품 중 하나이므로 물 분자로 들어가야합니다. H2O 앞에 "2"를 쓰면 CH4를 넣을 때마다 두 개의 H2O가 반환된다는 것을 나타냅니다.

방정식에는 여전히 작은 문제가 있습니다. 산소가 충분하지 않습니다. 4 개의 산소 원자가 나오지만 2 개만 들어갑니다. 그래서 모든 것은 여전히 불균형입니다. O2 앞에 "2"를 써서 반응에서 충분히 나오기 위해 두 개의 O2를 넣어야 함을 나타냅니다.
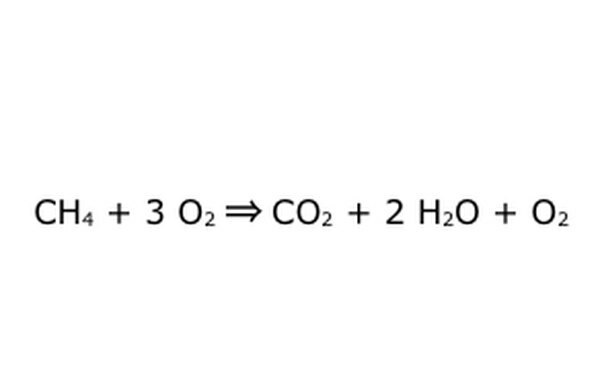
"과잉 산소에서"이와 같은 과정을 수행 할 수 있습니다. 이것이 의미하는 것은 방정식이 필요한 것보다 더 많은 산소를 투입하고 더 많은 것을 되 찾는다는 것입니다. 예를 들어, 여분의 O2가 들어가고 있으므로 여분이 나옵니다. 보존 법칙을 항상 준수해야합니다. 들어가는 것은 모두 나와야합니다.
팁
일반적으로 이러한 유형의 방정식에서 화학 물질은 몰 단위로 측정됩니다. 몰은 6.0221415 10 ^ (23) 분자를 나타내는 단위입니다. 이것은 이해하기에는 너무 큰 숫자이기 때문에 균형을 잡을 때 단일 분자로 생각하는 것이 더 쉽습니다. 시작할 때이 점에 유의하십시오.
